-
شماره تماس
-
آدرس آزمایشگاه
تهران، بلوار کاوه، خیابان بهار جنوبی،
بن بست تقوی، پلاک 14 -
ساعات کاری
شنبه تا چهارشنبه: 8:30 الی 20پنجشنبه ها: 8:30 الی 13
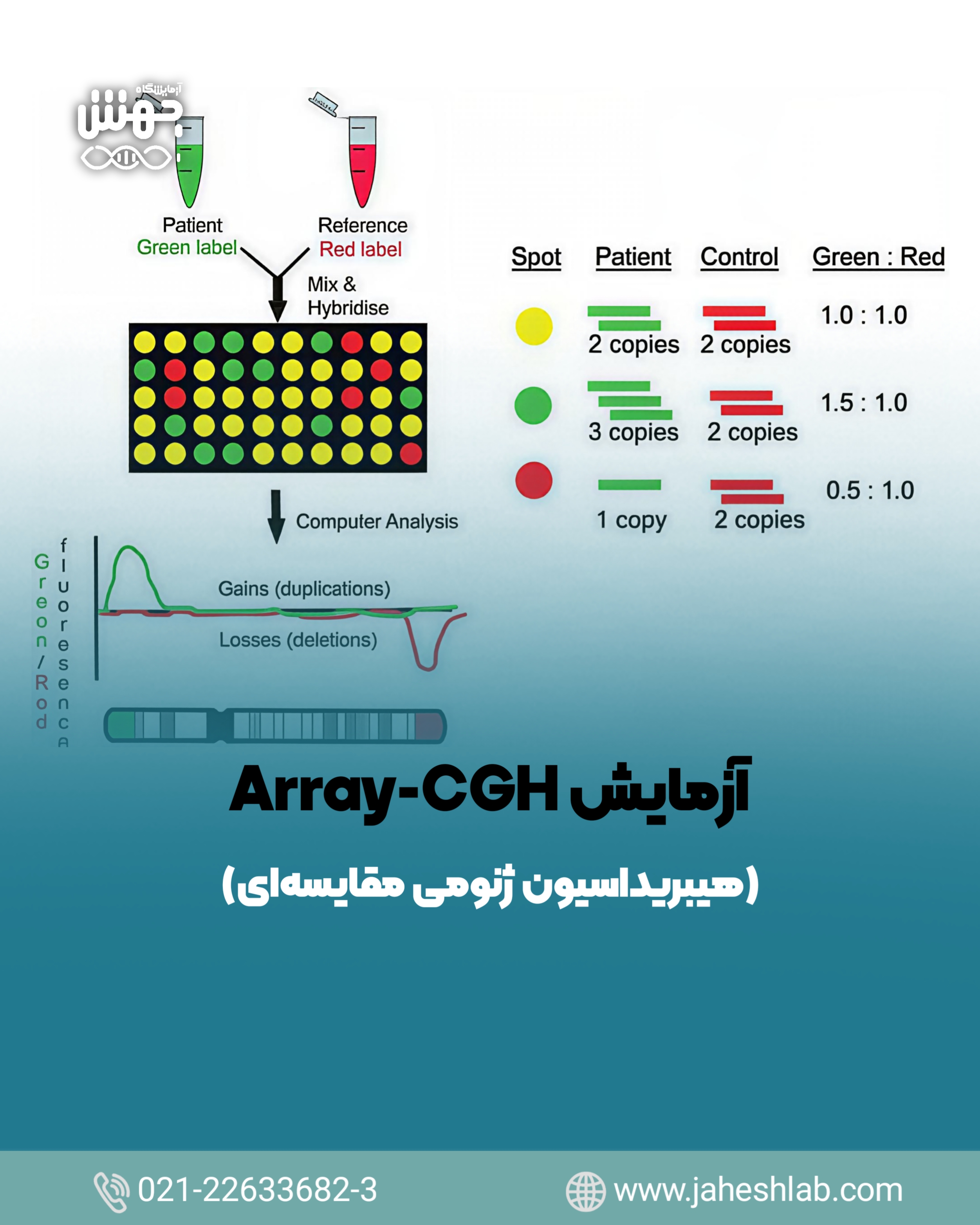
"Array CGH یک روش پیشرفته ژنومیک است که با مقایسه DNA بیمار و مرجع روی تراشهای با هزاران پروب، تغییرات دوز ژنومی (حذف یا افزونگی) را با وضوح بسیار بالاتر از کاریوتایپ (50-100 kb) شناسایی میکند و "کاریوتایپ مولکولی" تولید میکند."
آرایه CGH (هیبریداسیون ژنومی مقایسهای) امکان شناسایی تغییرات دز ژنومی حذف یا(duplicasion) را با سطح وضوحی بسیار بالاتر از کاریوتایپینگ فراهم میکند.
مزایا و معایب آرایه CGH
مزایای آرایه CGH
مزایای این تکنیک عبارتند از:
معایب آرایه CGH
معایب این تکنیک عبارتند از اینکه نمیتواند موارد زیر را شناسایی کند:
کاربردهای آرایه CHG
کاربردهای آرایه CHG پیش از تولد
آرایه CGH در تشخیص پیش از تولد استفاده میشود:
میکروآرایهها نرخ شناسایی تغییرات کروموزومی مرتبط را در بارداریهای پرخطر ۵-۱۰٪ و در بارداریهای کمخطر ۱-۲٪ افزایش میدهند. از آنجا که این تکنیکها (و همچنین اگزوم و ژنوم) گاهی واریانتهای با اهمیت نامعلوم (VUS) بیشتری را شناسایی میکنند، مهم است که یک متخصص حرفهای دادهها را تفسیر کند و به پزشک و/یا بیمار مشاوره دهد.
کاربردهای آرایه CGH پس از تولد
این تکنیک اولیه انتخابشده برای مطالعه بیماران مبتلا به موارد زیر است:
دلیل این امر نرخ بازده تشخیصی بالاتر (۱۵-۲۰٪) نسبت به کاریوتایپینگ است. تکنیک اخیر باید به عنوان نشانه اولیه برای مطالعه بیماران با الگوهای کروموزومی قابلشناسایی، موارد با سابقه خانوادگی جابهجاییهای کروموزومی و در مطالعه ناباروری و/یا سقطهای مکرر استفاده شود.
وضوح آرایه CGH چیست؟
در مقایسه با تجزیه و تحلیل کروموزومی متداول که حد تشخیص آن ۵ تا ۱۰ مگاباز است، آرایه CGH میتواند تغییرات نامتعادل ژنومی را با وضوح تشخیصی ۵۰ تا ۱۰۰ کیلوباز شناسایی کند. آرایههای CGH میتوانند برای پوشش هر ناحیه مورد علاقه طراحی شوند و وضوحهای متفاوتی را به دست آورند. سطح وضوح توسط اندازه پروب استفادهشده، فاصله ژنومی بین پروبها یا تعداد پروبها در آرایه تعیین میشود. این به چه معناست؟
هرچه قطعه DNA استفادهشده به عنوان پروب کوچکتر باشد و دو پروب متوالی به هم نزدیکتر باشند، وضوح بالاتر است. آرایه ۶۰k دارای ۶۰,۰۰۰ پروب یا الیگونوکلئوتید توزیعشده در سراسر ژنوم است.
آرایه CGH چگونه کار میکند؟
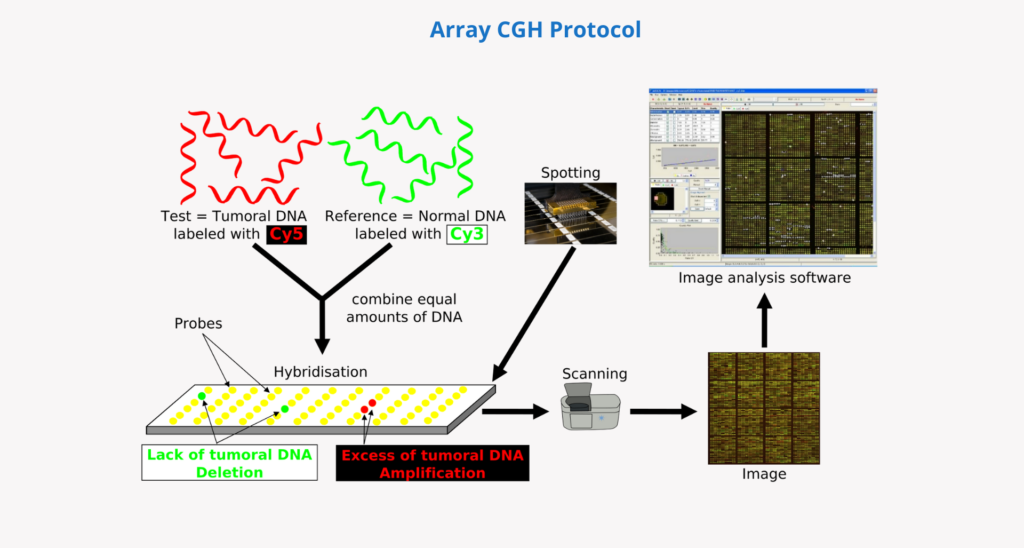
ابتدا DNA بیمار استخراج و هضم میشود (از نمونه خون، بزاق، پرزهای کوریونی، مایع آمنیوتیک یا سایر سلولها یا بافتها). سپس مقدار مساوی از DNA بیمار و DNA مرجع (کنترل) با فلوروفورهای متفاوت برچسبگذاری میشوند. آنها سپس مخلوط و دناتوره میشوند، از ساختار دو رشتهای به تکرشتهای.
در مرحله بعد، روی یک تراشه با قطعات DNA بیحرکت (پروبها) هیبرید میشوند. این پروبها ژنوم انسانی را تا حد ممکن به طور یکنواخت پوشش میدهند.
قطعات DNA بیمار و کنترل برای هیبریداسیون با توالیهای مکمل روی پروبهای آرایه رقابت میکنند. سپس یک اسکنر لیزری با وضوح بالا برای ثبت و کمیسازی شدت سیگنال فلورسنت هر رنگ که به هر پروب هیبرید شده، استفاده میشود.
در نهایت، نسبت شدت سیگنال فلورسنت در DNA بیمار و DNA مرجع برای هر پروب در آرایه محاسبه میشود و اطلاعاتی در مورد تعداد نسبی کپی توالیها در ژنوم بیمار در مقایسه با ژنوم مرجع به دست میآید. این اطلاعات توسط نرمافزار تفسیر میشود که اجازه میدهد دادهها به ناحیه کروموزومی مربوطه اختصاص یابد و به صورت «کاریوتایپ مولکولی» نمایش داده شود.
ساخته شده در آزمایشگاه جهش لب
نظر خود را قرار دهید